合成生物学底盘细胞之毕赤酵母
作者:聂荌 来源:网络 发布时间:2024-12-19 11:26阅读量:11231 会员投稿
酵母表达系统是真核表达系统中应用最广泛的之一,其中巴斯德毕赤酵母(Komagataella phaffii,又名Pichia pastoris)作为甲基营养型酵母的代表,近年来发展迅速,应用广泛。
毕赤酵母:基因表达的新纪元
毕赤酵母表达系统诞生于上世纪 80 年代初期,它融合了原核表达系统与真核表达系统的诸多优点,迅速在众多表达系统中脱颖而出。与原核表达系统相比,它不仅保留了操作简易、易于培养、生长速度快、表达量高、成本低等特性,还具备原核生物所欠缺的对外源蛋白的翻译后修饰能力,如糖基化、蛋白磷酸化等,使表达的重组蛋白更接近天然产物。同时,它又克服了酿酒酵母分泌效率差、表达菌株不稳定、表达质粒易丢失等缺陷,成为外源蛋白表达的理想选择。
毕赤酵母表达系统的主要优势
1. 高效AOX1启动子:目前最强、调控机制最严谨的启动子之一,便于调控外源基因的表达。
2. 蛋白加工修饰功能:可对表达的外源蛋白进行糖基化、磷酸化、脂类酰化等翻译后修饰,使重组蛋白与天然产物更相似。
3. 低成本与高效生长:菌株生长迅速,培养基成本低廉,培养条件简单。
4. 高表达量:外源蛋白表达量高,支持胞内和分泌表达。
5. 基因稳定整合:外源基因能在基因组的特定位点以单拷贝或多拷贝形式稳定整合,可稳定遗传50代以上。
6. 高密度发酵:耐受高密度发酵,便于工业化生产。
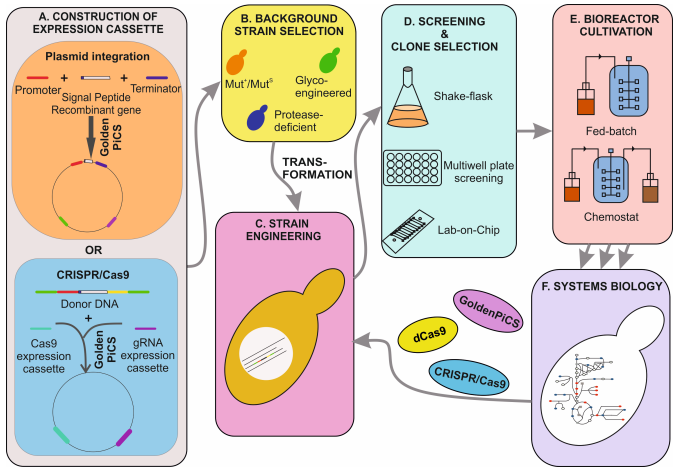
P. pastoris生产重组蛋白的流程
毕赤酵母菌株多样性
当前所采用的巴斯德毕赤酵母菌株都源自原始的Y-11430菌,常用的有GS115、KM71、X33和SMD1168等。蛋白胞内表达优先选MutS表型,分泌表达Mut + 和MutS均可;多数菌株如SMD1168、GS115、KM-71是组氨酸脱氢酶缺陷型,可用不含组氨酸培养基筛选重组子,且SMD1168为蛋白酶缺陷型,适合表达不稳定蛋白质或蛋白质复合物以避免内源性蛋白酶降解。但SMD1168菌株生长缓慢,导致蛋白质产量低
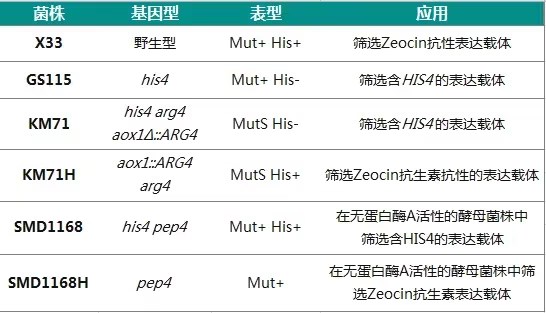
毕赤酵母常用表达载体
毕赤酵母表达载体分为分泌型和非分泌型两大类,分别适用于不同类型的蛋白质生产需求,其中分泌型载体利用酿酒酵母的分泌信号序列,有效引导外源蛋白的分泌,提高了蛋白的产量和纯度。因此,深入了解和优化毕赤酵母表达载体,对于提升蛋白生产效率和质量至关重要,也是当前生物技术和基因工程研究中的热点之一。
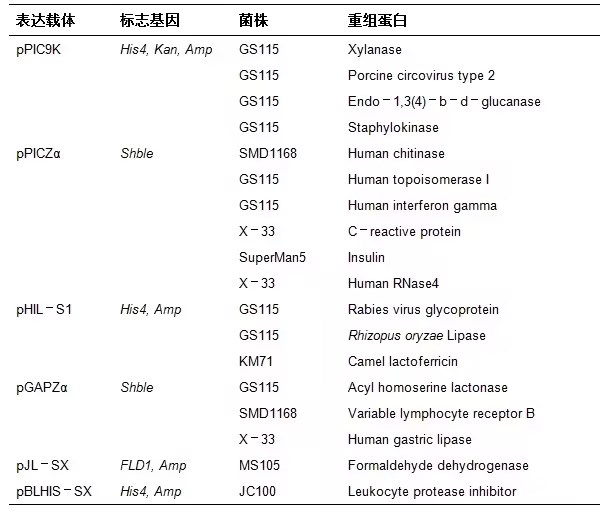
常见的用于生产分泌蛋白的毕赤酵母表达载体【1】
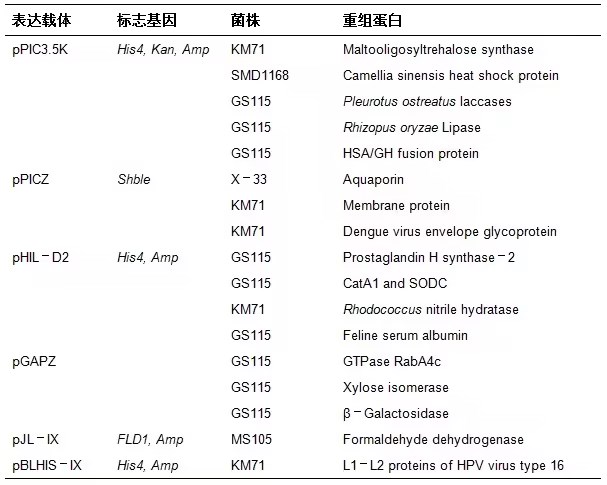
常见的用于生产胞内蛋白的毕赤酵母表达载体【1】
毕赤酵母基因改造技术
1. 基于线性化质粒载体的同源重组
同源重组技术是一种利用生物体自身修复机制的基因工程技术。在毕赤酵母中,通过将线性化的质粒载体引入,可以高效地将外源基因整合到宿主基因组的特定位点。这一过程依赖于同源臂序列,这些序列与目标基因组区域具有高度相似性,从而促进了质粒载体与宿主DNA之间的重组。这种方法的优势在于其操作简便、整合效率高,可以实现外源基因的多拷贝插入,这对于提高基因表达水平和蛋白质产量至关重要。在工业生产中,这种技术常被用于优化基因表达,以满足生物制药和工业酶生产的需求。此外,同源重组技术还可以用于基因功能研究、疾病模型构建以及生物技术产品的开发。
2. 基于CRISPR/Cas9的基因编辑
CRISPR/Cas9系统是一种革命性的基因编辑技术,它通过利用指导RNA(gRNA)引导核酸酶Cas9精确切割目标DNA序列。这种特异性的切割触发了细胞内的修复机制,包括非同源末端连接(NHEJ)和同源定向修复(HDR),从而实现基因的敲除、插入或替换。CRISPR/Cas9技术以其高效性和精准性在基因组编辑领域占据重要地位,特别适用于复杂代谢途径的优化和多基因编辑。在毕赤酵母中,CRISPR/Cas9技术已被广泛应用于基因功能研究、菌株改良以及生产性能的提升。例如,通过敲除或替换特定基因,可以增强宿主菌的蛋白质表达能力或改变其代谢特性,以适应特定的工业生产需求。
3. 基于CRISPR/Cas12的基因编辑
CRISPR/Cas12系统,也称为Cpf1,是CRISPR家族中的另一种基因编辑工具。Cas12蛋白具有广泛的靶向能力和单链DNA切割特性,使其在基因组编辑中具有独特的优势。与Cas9相比,Cas12对靶位点的PAM(原始间隔短回文重复序列)依赖性更宽松,这为基因编辑提供了更大的灵活性。CRISPR/Cas12系统在表观遗传调控和新型生物技术的开发中展现出巨大潜力,例如,它可以用于研究基因沉默、激活以及DNA甲基化等表观遗传修饰。此外,Cas12的单链切割特性使其在开发新型核酸检测技术、基因治疗策略以及合成生物学应用中具有独特的应用前景。在毕赤酵母中,CRISPR/Cas12技术的应用还相对较新,但已有研究表明,它在基因组编辑和基因功能研究中具有巨大的潜力。
毕赤酵母创新突破
经过几十年的广泛应用,毕赤酵母表达系统已成功表达了数以千计的异源蛋白,其中大部分为医药制品。美国 FDA 对该系统的认可,如 Cephelon 制剂的获批,充分证明了其安全性和有效性。在我国,虽然目前上市的基因工程药物大多源于大肠杆菌原核表达系统,但毕赤酵母表达系统凭借其国际上的广泛认可,必将在未来的医药市场中占据重要地位。
泓迅生物
酵母基因编辑 & 重组蛋白表达平台
泓迅生物利用CRISPR等新技术,实现了对毕赤酵母基因组的精准编辑,包括基因敲除、插入和替换。我们成功敲除了GS115菌株的KU70基因,显著提高了毕赤酵母的重组效率和外源基因的整合频率,同时敲除了pep4基因,降低了外源蛋白被降解的风险。
我们深耕合成生物学领域,拥有丰富的基因合成、重组蛋白表达和基因编辑经验。我们提供一站式解决方案,帮助解决毕赤酵母蛋白表达和基因改造的需求,最大限度缩短研发周期。
》案例展示
通过对毕赤酵母GS115的基因改造,提高了菌株对外源蛋白的表达和分泌。并利用该重组菌株成功表达了多个人源重组蛋白的高效分泌表达,培养液中杂蛋白很少,产量预计可达10g/L。

》免费样品测试
· 可免费提供少量蛋白样品以供测试。
· 菌株、蛋白等相关信息可联系泓迅生物咨询。
未来展望
毕赤酵母表达系统以其高表达、高密度、多样化翻译后修饰以及无内毒素和病毒的安全性等优势,成为重组蛋白表达的优选平台。CRISPR/Cas9等基因组编辑技术的应用将进一步推动该系统的发展,助力重组人源蛋白在生物医药、美容护肤等领域的研究和应用。
重组胶原蛋白基因的选择和设计、表达条件的优化和验证对于获得高产量的蛋白至关重要。泓迅生物提供从“序列优化”到“基因合成”到“重组胶原蛋白表达”一站式服务。高效的基因合成、多种表达体系协助您在实验室低成本无限合成,提高胶原蛋白的表达量、亲水性和可加工性,创造更多应用可能。
参考文献
[1] Karbalaei M, Rezaee S A, Farsiani H. Pichia pastoris: A highly successful expression system for optimal synthesis of heterologous proteins[J]. Journal of cellular physiology, 2020, 235(9): 5867-5881.
[2] De S, Mattanovich D, Ferrer P, Gasser B. Established tools and emerging trends for the production of recombinant proteins and metabolites in Pichia pastoris. Essays Biochem. 2021 Jul 26;65(2):293-307.
[3] Cos, O. et al. (2006). Microbial Cell Factories, 5, 1-20.
[4] Staley, C. A. et al. (2012). Gene, 496(2), 118-127.
[5] 覃晓琳 et al. (2010). 生物技术, 20(3), 4.
[6] 周则迅 & 袁汉英. (2000). 复旦学报:自然科学版(3), 264-268.
[7] Siegel, R. S. & Brierley, R. A. (1989). Biotechnology and bioengineering, 34(3), 403-404.
[8] Liu, Q. et al. (2019). Microbial cell factories, 18, 1-11.
郑重声明:此文内容为本网站转载企业宣传资讯,目的在于传播更多信息,与本站立场无关。仅供读者参考,并请自行核实相关内容。

